Несмотря на то, что вакцины, возможно, открывают миру путь к нормализации после пандемии, постоянно мутирующий вирус SARS-CoV-2 требует разработки эффективных лекарств. В новом исследовании, опубликованном в научном журнале Nature Microbiology, исследователи израильского Института Вейцмана вместе с партнерами из французского Института Пастера и Национальными институтами здравоохранения (NIH) США предлагают новый терапевтический подход к борьбе с печально известным вирусом.
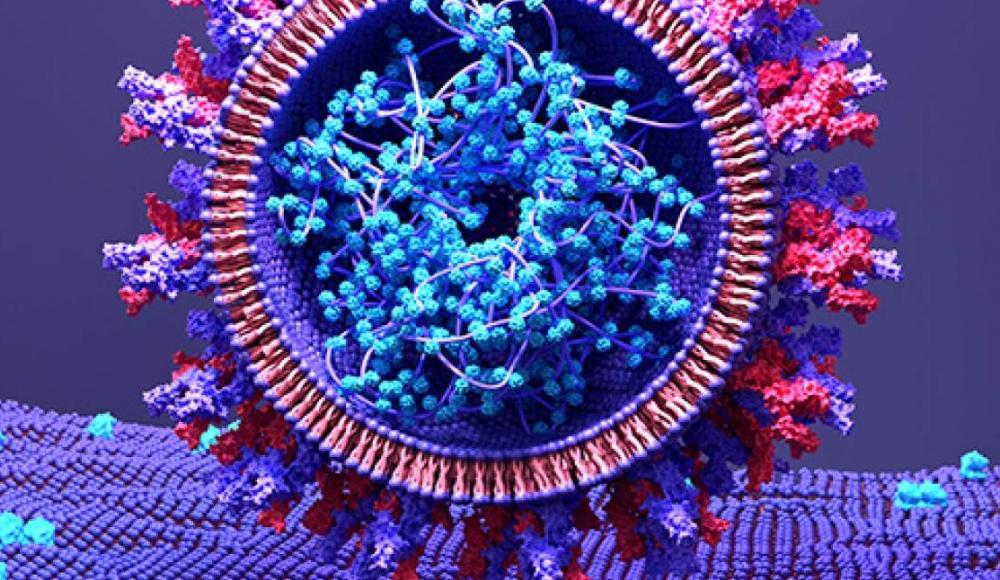
Вместо того, чтобы атаковать вирусный белок, ответственный за проникновение вируса в клетки организма человека, исследователи обратили свое внимание на белок мембраны наших клеток, который и "открывает" вирусу путь в клетку. Используя разработанный ими передовой метод искусственной эволюции, ученые создали молекулярную «суперпробку», которая физически блокирует это «входное отверстие», не позволяя вирусу прикрепиться к клетке и проникнуть в нее.
Большинство потенциальных методов лечения (и имеющихся вакцин) SARS-CoV-2 нацелены на так называемый «белковый шип» на внешней оболочке вируса. Однако этот белок подвержен мутациям, которые снижают эффективность имеющихся методов лечения. «Поскольку вирус постоянно развивается, мы решили вплотную заняться клеточным рецептором ACE2, который позволяет вирусу проникать в наши клетки, но сам не мутирует и не эволюционирует», - говорит руководитель исследования профессор Гидеон Шрайбер с отделения биомолекулярных наук Института Вейцмана. Этот подход может дать результаты, устойчивые к новым вариантам вируса.
ACE2, прикрепленный к мембране эпителиальных клеток легких и других тканей, является ферментом, важным для регуляции кровяного давления. Поэтому просто заблокировать этот рецептор, чтобы предотвратить проникновение SARS-CoV-2, нельзя - любая такая стратегия не должна мешать выполнению основной функции ACE2. Проф. Шрайбер, лаборатория которая специализируется на изучении взаимодействия между белками, решил разработать небольшую молекулу белка, которая могла бы связываться с ACE2 лучше, чем SARS-CoV-2, не влияя при этом на ферментативную активность рецептора.
Исследователи под руководством доктора Иржи Заградника, постдокторанта в группе Шрайбера, начали с определения "связывающего домена" SARS-CoV-2: относительно короткой последовательности строительных блоков в более крупном белке-шипе, который и связывается с ACE2. Используя собственный рецептор-связывающий домен вируса против него, Заградник провел несколько раундов «эволюции в пробирке» по методу, разработанному в лаборатории Шрайбера, на генетически модифицированном штамме обычных дрожжей. Поскольку дрожжами можно легко манипулировать, Заградник смог быстро сканировать миллионы различных мутаций, накопившихся в ходе этой искусственной эволюции, имитирующей естественную эволюцию, но в гораздо более быстром темпе. Целью процесса было найти небольшую молекулу, которая была бы значительно более «липкой», чем исходный вирус.
По ходу исследования были найдены убедительные доказательства гипотезы о том, что SARS-CoV-2 становится более заразным, когда мутации улучшают его соответствие ACE2. Уже после первого раунда отбора лабораторные варианты, более эффективно связывающиеся с ACE2, имитировали мутации, присутствующие в наиболее заразных штаммах SARS-CoV-2 - британский вариант (альфа), южноафриканский вариант (бета) и бразильский вариант (гамма). Интересно, что распространенный сейчас индийский вариант (дельта) использует другой метод, чтобы быть более заразным - он "научился" частично обходить иммунную систему человека.
В конце концов Заградник выделил небольшой фрагмент белка, обладающий способностью связывания в 1000 раз более сильной, чем у исходного связывающего домена. Эта «суперпробка» не только в точности подошла для ACE2 - как обнаружили аспирантки лаборатории Шрайбера Майя Шемеш и Шир Марциано, она еще и сохраняет его ферментативную активность. Благодаря столь сильному потенциалу связывания очень низкие концентрации вновь созданной молекулы оказались достаточны для достижения желаемого блокирующего эффекта.
Чтобы разработать потенциальный метод применения молекулы в качестве лекарственного средства, Шрайбер и его команда сотрудничали с профессором Иноном Рудихом с отделения наук о Земле и планетах Института Вейцмана. Вместе с доктором Айрой Мартоном и доктором Чунлин Ли они создали распылитель на основе аэрозоля, который позволит вводить разработанную молекулу пациентам путем обычной ингаляции.
На данный момент исследователи протестировали разработанную формулу в NIH на хомяках, инфицированных SARS-CoV-2. Предварительные результаты показывают, что новое лечение значительно снижает симптомы заболевания, что позволяет позитивно оценить его терапевтический потенциал. В ближайшем будущем в NIH планируется провести дополнительные доклинические исследования нового метода.