Исследователи Тель-Авивского университета определили новый генетический фактор риска сложного заболевания глаз AMD (возрастная дегенерация желтого пятна), которое считается основной причины потери зрения в пожилом возрасте.
Ученым удалось впервые опознать белки, играющие ключевую роль в развитии и функционировании ткани, поражаемой этим недугом, найти их точные участки в геноме и доказать связь между вариациями в этих геномных областях и риском развития AMD.
Исследованием руководили профессора Рут Эшери-Падан и профессор Ран Элькон и их сотрудники - Мазаль Коэн Гулкар, Наама Месика, Ахувит Давид и Май Эшель - с кафедры молекулярной генетики и биохимии человека на медицинском факультете Тель-Авивского университете. Результаты их работы опубликованы в журнале PLOS Biology.
Проф. Эшери-Падан: «Одной из самых серьезных проблем в генетических исследованиях сегодня является расшифровка генетических механизмов сложных заболеваний, вызванных комбинацией нескольких различных генетических факторов и факторов окружающей среды. Речь идет о диабете, болезнях кишечника, различных психических заболеваниях и других патологиях. К ним относится и болезнь AMD, которая вызывает дегенерацию центральной части сетчатки — основную причину потери зрения в пожилом возрасте в развитых странах».
«AMD имеет значительный генетический компонент. Исследования, сравнивавшие геномы людей с AMD и без нее, обнаружили различия в нескольких областях генома, вероятно, связанные с факторами риска развития AMD. Однако эти различия были обнаружены не в каком-либо конкретном гене, а скорее в обширных районах, объединяющих целый ряд генов, функции и способы работы которых до сих пор в значительной степени неизвестны. До сих пор никто не смог найти в этих участках генома специфические особенности, которые можно было бы определить как конкретный фактор риска. Наше исследование было направлено на решение этой проблемы».
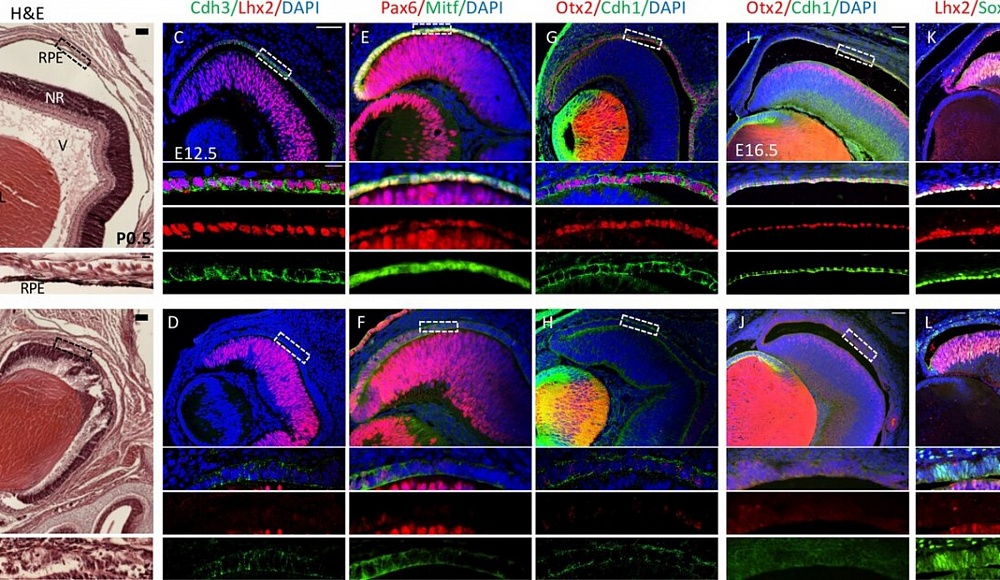
Ученые уделили особое внимание клеткам слоя ткани, называемого пигментированным эпителием сетчатки (ПЭС), который поддерживает фоторецепторы в сетчатке и необходим для их начального развития, а также для их выживания на протяжении всей жизни человека. По словам исследователей, именно эта ткань поражается AMD на самой ранней стадии болезни.
«Во-первых, мы хотели понять генетический механизм, который активирует и регулирует специфическую активность клеток пигментированного эпителия. В ходе серии экспериментов, убирая различные белки как в мышиной модели, так и в клетках человека, мы выявили два ключевых белковых соединения - LHX2 и OTX2 - которые вместе определяют экспрессию многих генов, уникальных для этой ткани. Белки действуют как активаторы транскрипции, связываясь со специфическими регуляторными участками в геноме, чтобы определить, какие гены будут "реализованы" в конкретной клетке».
Следующей задачей было определить точное расположение этих двух белков в геноме. Исследователи использовали инновационную технологию ChIP-seq — метод секвенирования ДНК, выявляющий точки, где белки связываются с ДНК. Проф. Элькон: «Мы обнаружили, что точки связывания двух белков были довольно близки друг к другу. Более того, эти же места в геноме оказались отмечены в ходе ранних исследований сравнения генома лиц с AMD и без нее (они находились среди выявленных аномальных участков генома пациентов с AMD).
Мы предполагаем, что из-за изменений в последовательностях ДНК в этих областях генома транскрипционные белки теряют способность эффективно закрепляться на своих точках связывания. Это, в свою очередь, снижает экспрессию соседнего гена, регулируемого этими белками, который и кодирует ионный канал, известный своей важностью для нормального функционирования нашего глаза. Снижение активности гена влияет на всю ткань, увеличивая риск развития AMD».
«Результаты нашей работы обеспечивают новый взгляд на нерешенную до сих пор проблему: функции и способ работы геномных последовательностей, расположенных вне генов, и их влияние на сложные генетические заболевания. Мы считаем, что наша новая методология позволит идентифицировать и "нанести на карту" многие другие генетические механизмы, связанные с AMD и другими комплексными генетическими заболеваниями».